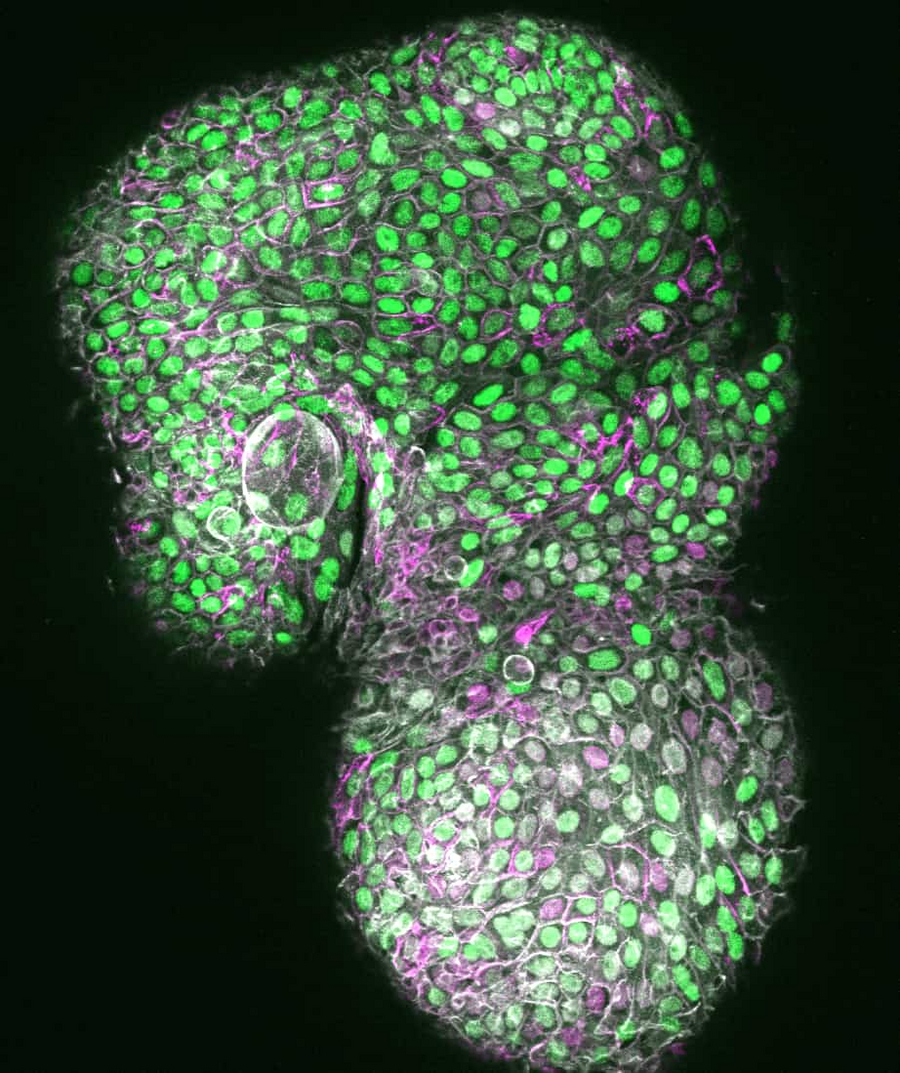
In dem optimierten Medium gezüchtete Leber-Ductus-Organoide weisen sowohl Cholangiozyten- (grün) als auch Hepatozyten- (magenta) Zellpopulationen auf. © Javier Bregante, Flaminia Kaluthantrige Don et al. Cell Reports, 2026 / MPI-CBG
Organoide sind dreidimensionale Modelle von Organen, die das entsprechende Organ in einem lebenden Organismus genau nachbilden. Sie bilden somit ein aussagekräftiges Versuchsmodell, mit dessen Hilfe sowohl Entwicklungs- als auch Krankheitsmechanismen besser verstanden werden können. Derzeit gibt es Organoide für fast alle Organe verschiedener Spezies, über die in den letzten zehn Jahren mehr als 20.000 wissenschaftliche Artikel veröffentlicht wurden.
Ein Großteil der menschlichen Leber besteht aus den beiden Zelltypen Hepatozyten und Ductuszellen (auch Cholangiozyten genannt). Bei schweren Leberschäden können Cholangiozyten, die in verschiedenen Zellzuständen vorkommen, sogar Hepatozyten ersetzen und tragen so entscheidend zur Reparatur der Leber bei. Bisher entwickelte Organoidmodelle waren jedoch nicht in der Lage, die Eigenschaften von Cholangiozyten zu reproduzieren. Daher war es bislang schwierig, die verschiedenen Arten von Cholangiozyten und die entsprechenden Lebererkrankungen zu verstehen.
Die Forschungsgruppe um Meritxell Huch, Direktorin am Max-Planck-Institut für molekulare Zellbiologie und Genetik (MPI-CBG) und Honorarprofessorin an der Medizinischen Fakultät der TU Dresden, hat kürzlich gemeinsam mit Mitarbeitenden des Universitätsklinikums Carl Gustav Carus und des Universitätsklinikums Rostock ein verbessertes Organoidmodell für menschliche Lebercholangiozyten entwickelt, mit dem die Cholangiozyten ihre Anpassungsfähigkeit und ihr Regenerationspotenzial in vitro zeigen können. Aufbauend auf ihren früheren Arbeiten zur Kultivierung von Cholangiozyten in einer Petrischale optimierten die Autoren die Kulturbedingungen, damit diese Cholangiozyten-Organoide das gesamte Spektrum der in der menschlichen Leber beobachteten Zellzustände darstellen können.
„Eine allgemeine Schwierigkeit bei der Erforschung von Organoiden besteht darin, das Gleichgewicht zwischen der Fähigkeit zur Zellvermehrung und der Vielzahl unterschiedlicher Zelltypen, die im tatsächlichen Organ vorkommen, aufrechtzuerhalten“, sagt Javier Bregante, Doktorand in der Huch-Gruppe und einer der Hauptautoren der in Cell Reports veröffentlichten Studie. „Wir haben dieses Problem gelöst, indem wir Wachstumsbedingungen für Organoide entwickelt haben, die die natürliche Umgebung des Gewebes besser nachahmen“, erklärt Flaminia Kaluthantrige Don, ehemalige Doktorandin derselben Gruppe und ebenfalls Hauptautorin der Studie.
Flaminia betont, dass das neue Modell das gesamte Spektrum der Cholangiozytenvielfalt erfasst und damit mechanistische Studien zur Leberreparatur und -regeneration sowie eine präzise Analyse der Signalwege ermöglicht, die Wachstum und Differenzierung regulieren. Meritxell Huch ergänzt:
Das System verbindet deskriptives Wissen über menschliche Leberzellen mit funktionellen Studien zur Physiologie und könnte auf patienteneigenes Material ausgeweitet werden, um krankheitsspezifische Veränderungen der Cholangiozytenfunktion zu untersuchen. Die Plattform ermöglicht erstmals die Analyse von Übergängen zwischen verschiedenen Zuständen menschlicher Cholangiozyten und liefert neue Erkenntnisse über ihre Rolle bei der Aufrechterhaltung des Gleichgewichts und bei Erkrankungen.
Javier Bregante, Flaminia Kaluthantrige Don, Fabian Rost, André Gohr, Germán Belenguer, Franziska Baenke, Dylan Liabeuf, Jessie Pöche, Clemens Schafmayer, Michaela Wilsch-Bräuninger, Sebastian Hinz, Kevin O’ Holleran, Daniel E. Stange, Meritxell Huch: Human liver cholangiocyte organoids capture the heterogeneity of in vivo liver ductal epithelium, Cell Reports, Volume 45, Issue 1, 2026, 116786.
https://doi.org/10.1016/j.celrep.2025.116786.