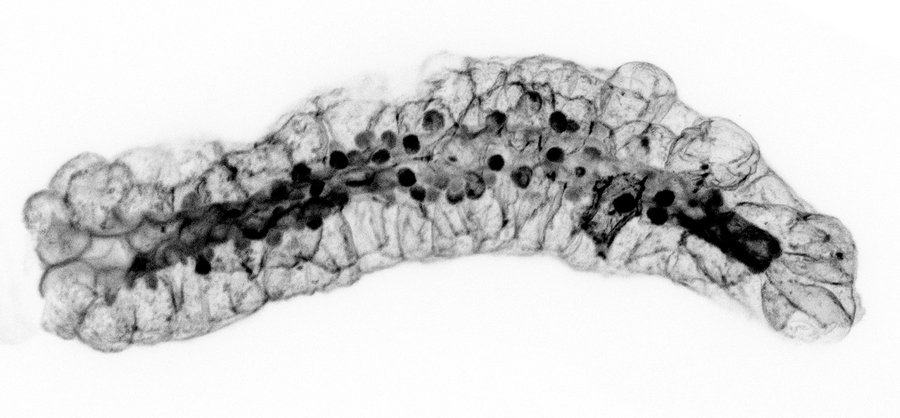
Speicheldrüse mit ungenügend Crumbs-Proteinen und ungewöhnlichen Lipidanreicherungen.© Lattner et al.
Ein reibungsloser Ablauf von Transportmechanismen innerhalb von Zellmembranen ist für das Funktionieren polarisierter Epithelzellen von großer Bedeutung. Sind diese Mechanismen defekt, werden sie mit einer Vielzahl von Krankheitsbildern verbunden, darunter Immunsyndrome, Taubheit, neuronale Degeneration und Krebs. Eine Forschungsgruppe aus dem Biotechnologischen Zentrum der TU Dresden (BIOTEC) und dem MPI-CBG in Dresden, hat deshalb untersucht, wie Polaritätsproteine den Transport innerhalb von Membranen regulieren.
Mithilfe der Speicheldrüse von Drosophila-Larven zeigten sie, dass das Schlüsselprotein Crumbs, welches für den Polaritätsprozess verantwortlich ist, außerdem die apikale Sekretionsmaschinerie organisiert. Die Ergebnisse deuten darauf hin, dass Crumbs für die Selbstregulation der Membran, die physiologische Funktion der Drüsen und durch diese Beeinflussung des Ernährungsverhaltens, auch für Entwicklung der Larven unerlässlich ist. Obwohl Crumbs bereits eine bekannte Schlüsseldeterminante der apikalen Plasmamembran ist, ist über den Mechanismus dahinter bisher nur sehr wenig bekannt. Diese Arbeit liefert einen molekularen Mechanismus, der erklärt, wie Crumbs die apikale Membranorganisation und Identität kontrolliert.
Die Studie liefert ein attraktives experimentelles Modell, um die molekularen Mechanismen hinter der Erhaltung polarisierter Membranen in vivo zu analysieren. Dies könnte helfen zu verstehen, wie Zellen den Transport und die Abgabe bestimmter Stoffe unter physiologischen Bedingungen und vor allem auch unter pathologischen Bedingungen kontrollieren. Beispielsweise deuten die Ergebnisse darauf hin, dass Crumbs und der Lipidregulator Pten an der Microvillus-Einschlusskrankheit (MVID) beteiligt sein könnten, einer tödlichen genetischen Krankheit, die durch den Mangel an Microvilli auf der Oberfläche von Enterozyten gekennzeichnet ist. Für sich anschließende Forschung wäre interessant, ob der hier beschriebene molekulare Mechanismus auch in das Krankheitsbild der mit Mutationen im menschlichen Gen CRUMBS1 verbundenen menschlichen Netzhautdegeneration involviert ist. Eine Mutation von der ungefähr 80.000 Menschen weltweit betroffen sind.
Johanna Lattner, Weihua Leng, Elisabeth Knust, Marko Brankatschk, David Flores-Benitez: "Crumbs organizes the transport machinery by regulating apical levels of PI(4,5)P2 in Drosophila". eLife, 7. November, 2019. DOI: 10.7554/eLife.50900