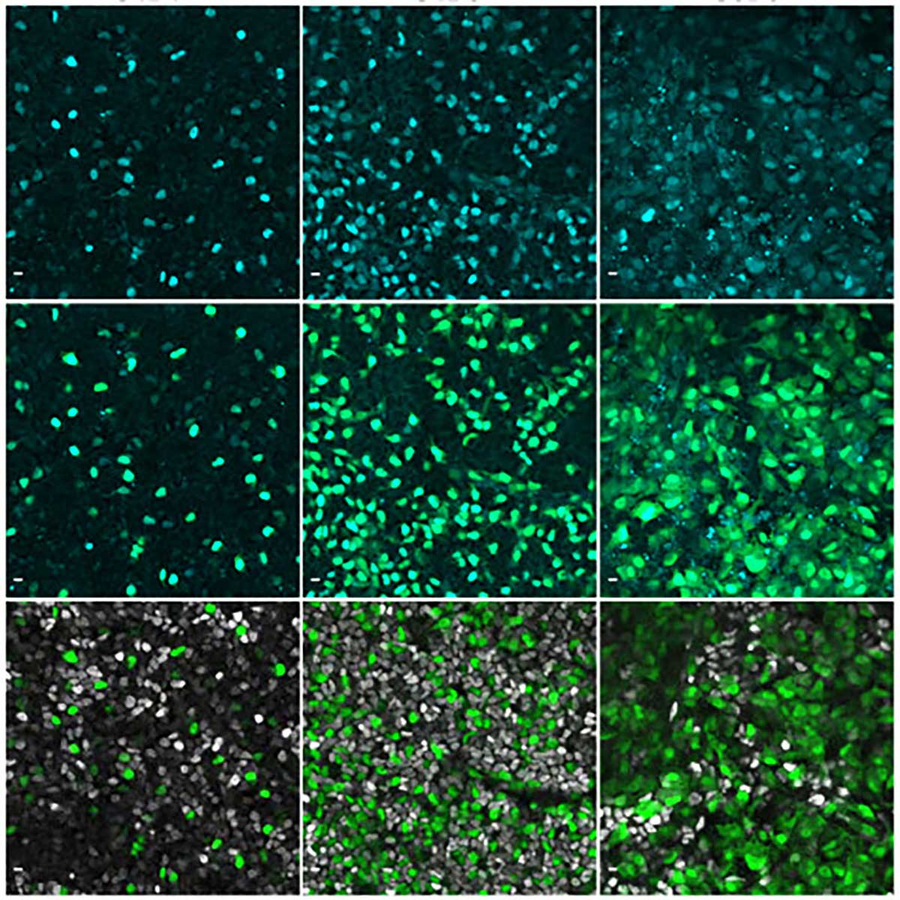
Immunofluoreszenzbilder zeigen das Gen NEUROG3 in Cyan in menschlichen Zellen der Bauchspeicheldrüse. © Beydag-Tasöz et al., Developmental Cell, MPI-CBG
Unsere Bauchspeicheldrüse besteht aus verschiedenen Zellen, die bei der Kontrolle unseres Blutzuckers sehr wichtig sind. Eines dieser Gene in den Pankreaszellen ist Neurogenin 3 (NEUROG3), dessen Mutation zu Diabetes führen kann. Dieses Gen ist während der Entwicklung der Bauchspeicheldrüse nur für kurze Zeit aktiv, weshalb dessen Verhalten und Dynamik insbesondere im Zusammenhang mit der menschlichen Entwicklung bisher ungeklärt war. Forschende des Max-Planck-Instituts für molekulare Zellbiologie und Genetik (MPI-CBG) in Dresden und der Novo Nordisk Foundation an der Universität Kopenhagen haben nun eine spezielle Methode verwendet, um sowohl die Aktivität des Gens als auch das Protein, das es in menschlichen Bauchspeicheldrüsenzellen bildet, zu beobachten und damit das Gen besser zu verstehen. Diese Methode ermöglicht es, das dynamische Verhalten von Bauchspeicheldrüsenzellen, welches in Live-Aufnahmen beobachtet werden konnte, mit allen von ihnen produzierten Genen zu verknüpfen. Dadurch lässt sich besser verstehen, wie sich die hormonproduzierenden Zellen der Bauchspeicheldrüse entwickeln. Dies könnte den Weg ebnen, um mehr dieser Zellen für therapeutische Zwecke zu gewinnen, beispielsweise für die Produktion und Transplantation dieser Zellen bei Patienten, die an Diabetes leiden.
Die unterschiedlichen Zellen in der Bauchspeicheldrüse kontrollieren unseren Blutzucker, wie zum Beispiel die Betazellen, die Insulin produzieren. Insulin hilft, unseren Blutzucker zu senken. Wenn diese Zellen nicht mehr funktionieren oder absterben, können wir an Diabetes erkranken. Während unseres Körperwachstums stammen alle diese speziellen Zellen von einem einzigen Zelltyp in der Bauchspeicheldrüse ab, dem endokrinen Vorläufer des Pankreas. Dieser Zelltyp nutzt nur für kurze Zeit ein Gen namens NEUROG3, um seine Aufgabe zu erfüllen.
Die Forschungsgruppe von Anne Grapin-Botton, geschäftsführende Direktorin am MPI-CBG in Dresden, hat sich zusammen mit Kollegen der Novo Nordisk Foundation an der Universität Kopenhagen zum Ziel gesetzt, diese besonderen Zellen in der Bauchspeicheldrüse, die das Gen NEUROG3 nutzen, genauer zu erforschen und zu verstehen, wie sich dieses Gen in einzelnen Zellen verhält.
“Wir haben spezielle Markierungen verwendet, um NEUROG3 in diesen Zellen zu sehen. So konnten wir in Live-Aufnahmen beobachten, wie sich die Zellen über einen längeren Zeitraum bewegen“, erklärt Belin Selcen Beydag-Tasöz, die Erstautorin der Studie, und fährt fort: „Indem wir 2-D- und 3-D-Modelle der menschlichen Bauchspeicheldrüse betrachteten, fanden wir heraus, dass die Konzentration des NEUROG3-Gens in den verschiedenen Zellen unterschiedlich war. Einige Zellen hatten viel von diesem Gen, andere nur wenig. Überraschenderweise bildeten alle Zellen, in denen NEUROG3 nachweisbar war, trotz dieser Unterschiede Zellen, die Hormone produzieren. Ein anderes überraschendes Ergebnis war, dass NEUROG3 bei Menschen etwa zweimal langsamer arbeitet als bei Mäusen. Das bedeutet, dass dieses Gen bei Menschen mehr Zeit braucht, um seine Aufgabe zu erfüllen als bei Mäusen.”
Das Team nutzte die Methode der Langzeit-Live-Bildgebung, um einen Prozess zu beobachten, der normalerweise im Mutterleib verborgen bleibt. Die Helligkeit der Zellen half ihnen, die Aktivität der Gene mit dem Verhalten der Zellen zu kombinieren. Auf diese Weise fand das Forschungsteam heraus, dass ein anderes Gen namens KLK12 dafür sorgt, dass die Zellen sich bewegen, um Langerhans-Inseln zu bilden, sobald das NEUROG3-Gen zu arbeiten beginnt.
Anne Grapin-Botton, die die Studie leitete, fasst zusammen: „Die Zellkultursysteme, die wir entwickelt haben, um zu verstehen, wie Zellen in menschlichen Embryonen Organe bilden, tragen erste Früchte. In unserer Studie haben wir wesentlich mehr über die Art und Weise gelernt, wie die Aktivität bestimmter Gene während der embryonalen Entwicklung zu Diabetes im späteren Leben führen kann. Die Ergebnisse zeigen, dass man bei der Herstellung von endokrinen Zellen für künftige therapeutische Anwendungen, bei denen diese Zellen Diabetikern transplantiert werden, eine gewisse Flexibilität hinsichtlich der Kontrolle von NEUROG3 hat.“
Belin Selcen Beydag-Tasöz, Joyson Verner D’Costa, Lena Hersemann, Byung Ho Lee, Federica Luppino, Yung Hae Kim, Christoph Zechner, Anne Grapin-Botton: Integrating single-cell imaging and RNA sequencing datasets links differentiation and morphogenetic dynamics of human pancreatic endocrine progenitors, Developmental Cell, 2023, https://doi.org/10.1016/j.devcel.2023.07.019.
Wissenschaftlicher Kontact:
Dr. Anne Grapin-Botton
+49 (0) 351 210-2500
botton(at)mpi-cbg.de
Pressekontakt MPI-CBG
Katrin Boes
+49 (0) 351 210-2080
kboes(at)mpi-cbg.de